Основные положения МКТ
Главное положение молекулярно-кинетической теории молекул
- Все природные вещества могут находиться в жидком, твердом или газообразном состоянии, в зависимости от внешних условий и особенностей.
- Все вещества образуются из частиц, которые в свою очередь состоят из атомов.
- Элементарные молекулы могут быть представлены сложным строением, а именно, наличие в своем составе нескольких молекул.
- Молекулы и атомы – это электрически нейтральные частицы. Они в конкретных определенных условиях способны приобретать дополнительный электрический заряд частиц и далее переходить в ионы положительного или отрицательного значения.
- Движение атомов и молекул, всегда происходит в непрерывном процессе.
- Частицы с электрической природой силы всегда, имеют свойство, взаимодействовать друг с другом.

Основное положение и суть молекулярно кинетической теории подтверждает Броуновское движение молекул. Также данное движение опытно обосновывает основное положение. Тепловое движение частиц осуществляется с молекулами, которые являются взвешенными в жидкой и газообразной среде вещества.
Опытное обоснование основных положений молекулярно кинетической теории
В 1827 году ученый Р. Броун сделал открытие, относительно движения, которое было обусловлено ударами беспорядочного типа и перемещениями молекул частиц. Данный процесс осуществлялся хаотично, и удары не могли уравновешивать друг друга. Следовательно, что скорость Броуновской частицы не может быть постоянным значением. Ей свойственно постоянное изменение, а движение направления имеет зигзагообразную форму, которая отображена на рисунке 1.
О броуновском движении неоднократно упоминал еще А. Эйнштейн в 1905 году. Его теория нашла подтверждение в практических опытах Ж. Перрена в период с 1908 по 1911 годов.
Из теории Эйнштейна есть следующее свойство: квадрат смещения < r 2 > броуновской частицы относительно первоначального положения, усредненное по многим броуновским частицам, является пропорциональным относительно времени наблюдения равным t.
Выражение, которое обозначается как < r 2 > = D t характеризует диффузионный закон. Относительно теории имеем, что D будет монотонно возрастать при процессе увеличения температурных показателей.
Движение в хаотичном порядке будет происходить при наличии диффузии.
Диффузия – это определение явления, при котором происходит проникновение двух или нескольких веществ соприкасающихся между собой, в друг друга.
Такой процесс в основном происходит достаточно быстротечно, и в газообразной среде.
Используя примеры диффузии с различными по плотности составами, можно получить смесь однородного типа.
При расположении в одном сосуде двух химических веществ: кислорода O2 и водорода H 2Р2 с перегородкой, будет происходить следующая реакция. Если удалить перегородку, газы постепенно будут смешиваться, тем самым образуя опасную химическую смесь.
Такой процесс возможен, если водород находится сверху, а кислород внизу.
В жидкой среде, также могут протекать процессы взаимопроникновения, однако это происходит значительно медленней.
При растворении твердого тела, сахара, в воде, то можно получить однородный раствор. Следовательно, он будет являться наглядным примером диффузионных процессов в жидком веществе.
Для реальных условий перемешивание в жидкости или газообразной среде замаскировано быстрыми процессами движения и преобразования.
Например: возникновение и образование конвекционных потоков.
Для диффузии твердых тел отличительной чертой является замедленное действие при перемещении.
Если поверхность взаимодействия металлов почистить, то можно рассмотреть следующий момент. При истечении большого временного периода, в каждом из металлов могут образовываться атомы других металлов.
Два движения, диффузное и броуновское, в науке принято считать равными друг для друга.
При взаимопроникновении частиц любых двух веществ, движение осуществляется беспорядочно и хаотично. Следовательно, наблюдается хаотичное тепловое перемещение молекул.
Принцип и применение Броуновского движения
Силы, которые действуют между двумя молекулами, всегда зависят от расстояния между ними же.
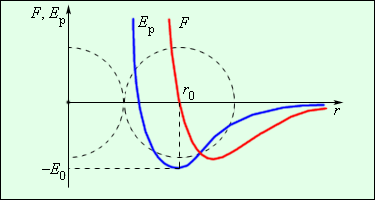
Молекулы имеют в своем составе, как положительные, так и отрицательные частицы. Если расстояния между молекулами большое, то будут преобладать межмолекулярное притяжение. Когда будет наблюдаться обратный эффект, а именно малые расстояния, то силы будут иметь отталкивающий характер.
На выше расположенном рисунке, можно наблюдать зависимость силы F и потенциальной энергии Ер, также взаимодействие между молекулами от расстояния от центра их расположения.
Если расстояние равно r = 0, то взаимодействующую сила обращается в нулевой показатель. Такое расстояние условно принимают в качестве показателя диаметра молекулы. При r = r0 потенциальная энергия взаимодействия принимает минимальный числовой показатель..
Чтобы отдалить две молекулы с расстоянием r 0 , следует сообщить E 0 , называемую энергией связи или глубиной потенциальной ямы.
С учетом того, что молекулы имеют малые размеры и параметры, простые одноатомные могут быть размером 10–10 м. Более сложные способны достигать размеров в несколько сот раз более.
Тепловое движение — это беспорядочный и хаотичный процесс движения молекул.
При увеличении показателей температуры, будет увеличивается кинетическая энергия всего теплового движения. Когда температура низкая, то средняя кинетическая энергия, будет оказывать наиболее меньшее значение глубины потенциальной ямы E0. Данный момент указывает, что все молекулы перетекают в жидкое или твердое вещество с расстоянием, имеющим средний показатель.
Когда температура начинает повышаться, то средняя кинетическая энергия молекулы существенно превышает E0. Следовательно, молекулы начинают процесс разлета и образуют вещество газообразного типа.
В твердых телах молекулы двигаются беспорядочно около фиксированных центров, то есть, положений равновесия. В пространстве может быть распределены нерегулярным образом (у аморфных тел) или с образованием упорядоченных объемных структур (кристаллических тел).

Нет времени решать самому?
Наши эксперты помогут!
Контрольная
| от 300 ₽ |
Реферат
| от 500 ₽ |
Курсовая
| от 1 000 ₽ |
Агрегатные состояния, которые могут приобретать вещества
Свободный процесс теплового движения молекулярных частиц, будет просматриваться в жидкой среде. Это происходит по причине отсутствия привязки их к центрам, и позволяет перемещаться по всему заданному объему.
Такой характер движения, объясняется текучестью вещества.
Если молекулы находятся близко, возможно образование упорядоченных структур с несколькими молекулами. Такое явление получило название ближнего порядка. Данный порядок более распространен, для тел кристаллического строения.
В газовой среде расстояние между молекулами намного больше, чем в иной среде. Поэтому действующие силы имеют малые показатели, а их движения происходят вдоль прямой, при этом оживая очередного соударения друг с другом.
Значение 10 – 8 является средним показателем для расстояния между молекулами воздуха в нормальных условиях. Так как, взаимодействие сил слабое, газы расширяются и способны наполнить любой сосуд и разного объема. Когда их взаимодействие стремится к нулю, то говорят о представлении идеального газа в среде.
Кинетическая модель для идеального газового вещества
В молекулярной кинетической теории состав и количество веществ всегда принимается пропорциональным общему числу частиц.
Моль — это объем вещества, которое содержит столько частиц, сколько содержится атомов в 0,012 кг углеродного вещества. Молекула данного вещества включает в себя один атом. Следовательно, одна моль вещества имеет одинаковое количество молекул. Такое число в науке называют Авогадро NA=6,02с1023 моль 01
Масса одного моля вещества — это молярная масса, которая имеет обозначение М. Она определяется по следующей формуле:
\[\mathrm{M}=\mathrm{NA} \mathrm{cm}_{0}\]
Выражается молярная масса показателем в килограммах на моль.